很多人都知道经颅磁刺激可以用于治疗,却忽略了其检测方面的强大功能。那么经颅磁刺激到底是怎么实现检测功能的呢?经颅磁刺激有多种脉冲形式,包括单脉冲刺激、成对脉冲刺激、重复脉冲刺激rTMS、TBS模式及其他刺激模式等。其中用于检测的主要是单脉冲刺激模式和成对脉冲刺激模式。
u 单脉冲刺激(single-pulse TMS,sTMS)
指每次输出一个脉冲刺激,可用于患者初次治疗前静息或活动运动阈值(MT)、运动诱发电位(MEP)、中枢传导时间(CMCT)、皮质静息期(CSP)等检测。
u 成对脉冲刺激(paired-pulse TMS,pTMS也可写成ppTMS)
成对TMS(pTMS)是指具有锁时关系的两个脉冲刺激,两个脉冲成对出现,两脉冲间通过时间间歇(ISI)不同产生不同的生物学效应,ISI通常从0到50ms可调。
第一个脉冲称为条件刺激(conditioning TMS,CS),多置于对侧运动皮质、小脑,第二个脉冲称为实验刺激(test TMS,TS),多置于运动皮质处且多为阈上刺激。成对脉冲刺激若两个脉冲在一个刺激线圈中输出,作用于一个部位,可实施的检测项目有皮层内抑制(ICI)和皮层内易化(ICF),ICI包含短时程皮层内抑制(SICI)、长时程皮层内抑制(LICI)。
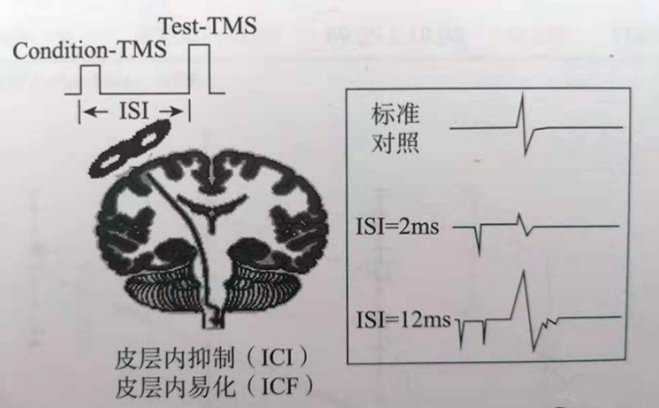
若在两个刺激线圈中输出,每个线圈各一个脉冲,可实行两皮质间的关联刺激(ccPAS)、两半球间的成对刺激如半球间抑制(IHI)。
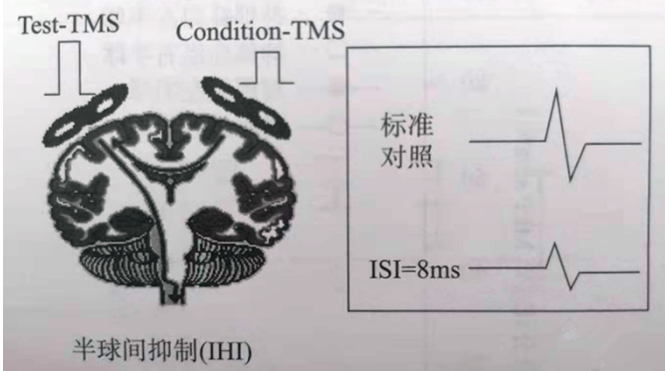
单脉冲是成对脉冲刺激的应用基础,成对脉冲刺激应用于检测时依赖于单脉冲刺激。成对脉冲刺激应用于检测时往往利用单脉冲刺激先进行MEP的检测,再进行成对脉冲刺激,记录相应的MEP图形,将pTMS的MEP波形与sTMS的MEP波形数据进行比较分析,以便了解条件刺激对试验刺激产生的影响,可用于健康人群以及患病人群的检测(排除禁忌症之外)。那在临床和科研中应用最为广泛的运动诱发电位检测是怎么实现呢?
受试者取坐位,右手掌向上,呈自然放松状态,置于右腿上,刺激线圈放置于左侧手“运动热点”处(运动热点是指最容易引出运动诱发电位的脑皮层处),以单脉冲刺激模式刺激“运动热点”,采用磁场刺激仪自带的 MEP 功能模块记录运动诱发电位(MEP)。
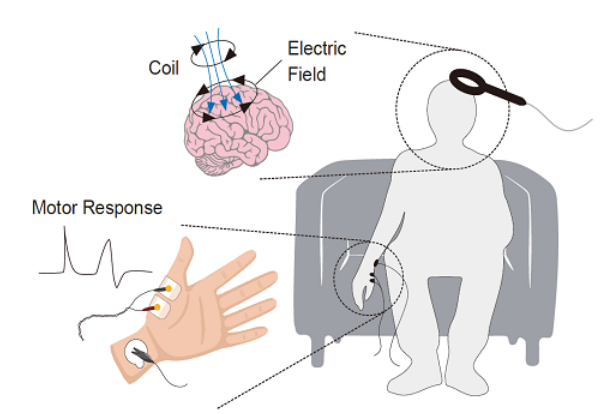
测试时记录电极置于拇短展肌肌腹;参考电极置于拇短展肌肌腱(骨性突起处),记录电极与参考电极一般相距约2-3cm;地线置于刺激部位与记录电极之间(手腕处),以减少刺激伪迹;注:当刺激部位发生变化时相应脑皮质区域、记录电极位置、参考电极位置以及底地线位置应进行调整(如当刺激下肢皮质功能区时,记录电极可粘贴于胫骨前肌表面皮肤,地线可置于踝部)。通过不断调节sTMS刺激强度和观察MEP波幅,10 次中有5次能采集到约 50μV波幅时的最小强度即为左侧M1 静息运动阈值(rMT)。
运动阈值属于运动诱发电位中的特例,常规运动诱发电位的刺激强度多以运动阈值为参考,《国际TMS诊断指南》中提出做常规MEP时可采用170% rMT的强度进行刺激。 具体操作
sTMS在临床的应用(以运动阈值测定为例)
由于治疗强度是以阈值作为参考而确定的,通常为80%-120% rMT,而个体的阈值多不相同,所以,用sTMS进行阈值检测是所有临床治疗和科研前必须进行的项目。
早在1995年,E. M. Khedr在研究重复经颅磁刺激对帕金森病患者运动功能的影响中,在首次rTMS刺激前也利用sTMS进行了运动阈值的测量。Vallsole等也通过单脉冲刺激观察到帕金森患者在静息时其 MEP波幅上升,同时还强调MEP的波幅在活动时上升的幅度较正常对照组低[1]。在对单侧大脑半球卒中后患者吞咽障碍的患者进行高频重复治疗前也同样利用了单脉冲刺激进行了阈值的测量,并依此确定治疗强度[2]。
pTMS在临床的应用(以皮层内抑制或易化为例)
皮层内抑制和易化是pTMS在健康人群或神经性疾病中常用的一种科研及临床检测指标。Florinda等使用EEG-pTMS作用于8例健康志愿者左侧初始运动皮层,并分别进行亚阈值、超阈值单次刺激和pTMS刺激(成对刺激采用3ms SICI和11ms ICF),结合脑电图分析,证明EEG-pTMS是一种很有前景的工具,可以更好地描述皮层下神经回路有效的连通性以及调节人类皮层和皮质脊髓通路中抑制和促进之间的平衡的机制[3]。在评估不同病情和脑卒中后不同时期患者健侧和患侧半球兴奋性的变化时,2018年有学者也利用了pTMS(条件刺激和实验刺激强度分别为静息运动阈值的80%和120%,且刺激间隔采用3ms和10ms),研究了103例脑卒中患者在急性期和亚急性期内皮层内抑制(ICI)和皮层内内易化(ICF)情况[4]。

可实现双部位检测和治疗的MagTD系列磁场刺激仪
在研究棕榈酰乙醇胺联合叶黄素对额颞叶痴呆患者额叶功能、高频振荡和GABA能传递的影响时,Assogna等人也同样也利用了pTMS来评估长时程增强(LTP)样皮质可塑性、短间隔皮层内抑制(SICI)、长间隔皮层内抑制(LICI)和短延迟传入抑制[5]。同样,在神经性疼痛方面的研究中,J.-P. Lefaucheur也利用单脉冲和pTMS研究14例慢性顽固性神经性疼痛患者治疗前和治疗后的皮层兴奋性,并以2、3和4ms的刺激间隔(ISI)评估SICI情况,以10、12、15 ms的ISI评估皮层内易化(ICF)情况[6]。
【分中心招募】磁刺激检测正常人神经传导功能多中心临床研究招募通知
▼ 参考文献
[1] VallsSolé J, Pascualleone A , Wassermann E M , et al. Human motor evoked responses to paired transcranial magnetic stimuli.[J]. Electroencephalography & Clinical Neurophysiology/evoked Potentials, 1992, 85(6):355-364.[2] 欧阳瑶;朱其秀;阎文静;柳希芹;仪文斌;宋金花;韩婕;伊传建;高频重复经颅磁刺激对单侧大脑半球卒中后患者吞咽障碍的影响[J];中华物理医学与康复杂志;2019年04期.[3] Ferreri, F., Pasqualetti, P., Maatta, S., Ponzo, D., Ferrarelli, F., Tononi, G., … Rossini, P. M. (2011). P26.1 Human brain connectivity during single and paired pulse transcranial magnetic stimulation. Clinical Neurophysiology, 122, S179. doi:10.1016/s1388-2457(11)60645-7[4] Seo H Y , Kim G W , Won Y H , et al. Changes in Intracortical Excitability of Affected and Unaffected Hemispheres After Stroke Evaluated by Paired-Pulse Transcranial Magnetic Stimulation[J]. Annals of Rehabilitation Medicine, 2018, 42(4):495-501.[5] Assogna, M., Casula, E. P., Borghi, I., Bonnì, S., Samà, D., Motta, C., … Koch, G. (2020). Effects of Palmitoylethanolamide Combined with Luteoline on Frontal Lobe Functions, High Frequency Oscillations, and GABAergic Transmission in Patients with Frontotemporal Dementia. Journal of Alzheimer’s Disease, 1–12. doi:10.3233/jad-200426.[6] Lefaucheur, J.-P., Ayache, S. S., Sorel, M., Farhat, W. H., Zouari, H. G., Ciampi de Andrade, D., … Goujon, C. (2012). Analgesic effects of repetitive transcranial magnetic stimulation of the motor cortex in neuropathic pain: Influence of theta burst stimulation priming. European Journal of Pain, 16(10), 1403–1413. doi:10.1002/j.1532-2149.2012.00150.x
以上内容由依瑞德临床医学中心翻译整理,有不足之处请指正,转载请注明出处。